La glucólisis está presente en la mayoría de los organismos vivos. Es el primer paso en la respiración celular. Es una vía glucolítica, que conduce a una descomposición parcial de la glucosa en piruvato. La glucólisis es la vía común tanto en la respiración aeróbica como en la anaeróbica.
Es la vía central del catabolismo de la glucosa en la que la glucosa (compuesto de 6 carbonos) se convierte en piruvato (compuesto de 3 carbonos) a través de una secuencia de 10 pasos.
La glucólisis tiene lugar tanto en organismos aeróbicos como anaeróbicos y es el primer paso hacia el metabolismo de la glucosa.
La secuencia de reacciones glucolíticas difiere de una especie a otra en el mecanismo de su regulación y el destino metabólico posterior del piruvato formado al final del proceso.
En los organismos aeróbicos, la glucólisis es el preludio del ciclo del ácido cítrico y la cadena de transporte de electrones, que juntos liberan la mayor parte de la energía contenida en la glucosa.
También se le conoce como Embden-Meyerhof-Parnas o vía EMP, en honor a los trabajadores pioneros en el campo.
¿Ocurre la glucólisis en humanos?
Sí, la glucólisis ocurre en todas las células vivas, incluidos los humanos, durante la respiración celular. Es un proceso esencial para generar energía para realizar funciones metabólicas.
La glucólisis ocurre tanto en la respiración aeróbica como en la anaeróbica y se produce en el citoplasma de células procariotas y células eucariotas.
Es el proceso de catabolismo de la glucosa, donde la glucosa se oxida parcialmente para formar dos moléculas de ácido pirúvico. En los seres humanos, el ácido pirúvico producido en la glucólisis entra en el ciclo de Krebs para la oxidación completa y la producción de energía.
¿Cuales son las enzimas de glucólisis?
En la mayoría de los tipos de células, las enzimas que catalizan las reacciones glucolíticas están presentes en la fracción extramitocondrial de la célula en el citosol.
Una característica común en todas las enzimas involucradas en la glucólisis es que casi todas requieren Mg 2+ . Las siguientes son las enzimas que catalizan diferentes pasos a lo largo del proceso de glucólisis:
- Hexoquinasa
- Fosfoglucoisomerasa
- Fosfofructoquinasa
- Aldolasa
- Isomerasa de fosfotriosa
- Gliceraldehído 3-fosfato deshidrogenasa
- Fosfoglicerato quinasa
- Fosfoglicerato mutasa
- Enolasa
- Piruvato quinasa
¿Cuales son los pasos de la glucólisis?
Los diez pasos de la glucólisis ocurren en la siguiente secuencia:
Paso 1- Fosforilación de glucosa

- En el primer paso de la glucólisis, la glucosa se inicia o ceba para los pasos siguientes mediante fosforilación en el carbono C 6 .
- El proceso implica la transferencia de fosfato del ATP a glucosa formando Glucosa-6-fosfato en presencia de la enzima hexoquinasa y glucocinasa (en animales y microbios).
- Este paso también va acompañado de una considerable pérdida de energía en forma de calor.
Paso 2- Isomerización de glucosa-6-fosfato

- La glucosa 6-fosfato se isomeriza reversiblemente a fructosa 6-fosfato por la enzima fosfohexoisomerasa / fosfoglucoisomerasa.
- Esta reacción implica un cambio del oxígeno del carbonilo de C1 a C2, convirtiendo así una aldosa en una cetosa.
Paso 3- Fosforilación de fructosa-6-fosfato

- Este paso es el segundo paso inicial de la glucólisis, donde la fructosa-6-fosfato se convierte en fructosa-1,6-bisfosfato en presencia de la enzima fosfofructoquinasa.
- Al igual que en el Paso 1, el fosfato se transfiere del ATP mientras que también se pierde cierta cantidad de energía en forma de calor.
Paso 4- Escisión de fructosa 1, 6-difosfato
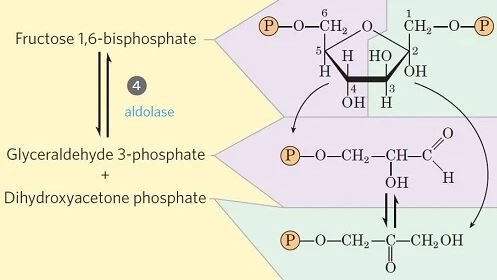
- Este paso implica la escisión única del enlace CC en la fructosa 1,6-bisfosfato.
- La enzima fructosa difosfato aldolasa cataliza la escisión de la fructosa 1,6-bisfosfato entre C 3 y C 4 dando como resultado dos triosa fosfatos diferentes: gliceraldehído 3-fosfato (una aldosa) y dihidroxiacetona fosfato (una cetosa).
- Los pasos restantes en la glucólisis involucran unidades de tres carbonos, en lugar de seis unidades de carbono.
Paso 5- Isomerización de fosfato de dihidroxiacetona
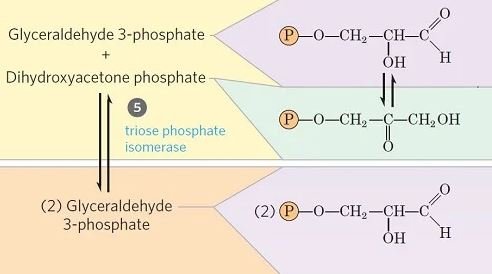
- El gliceraldehído 3-fosfato se puede degradar fácilmente en las etapas posteriores de la glucólisis, pero el fosfato de dihidroxiacetona no puede serlo. Por lo tanto, se isomeriza en su lugar en gliceraldehído 3-fosfato.
- En este paso, el fosfato de dihidroxiacetona se isomeriza en gliceraldehído 3-fosfato en presencia de la enzima triosa fosfato isomerasa.
- Esta reacción completa la primera fase de la glucólisis.
Paso 6- Fosforilación oxidativa de gliceraldehído 3-fosfato

- El paso 6 es uno de los tres pasos de formación o conservación de energía de la glucólisis.
- El gliceraldehído 3-fosfato se convierte en 1,3-bisfosfoglicerato por la enzima gliceraldehído 3-fosfato deshidrogenasa (fosfogliceraldehído deshidrogenasa).
- En este proceso, el NAD + se reduce a coenzima NADH por el H – del gliceraldehído 3-fosfato.
- Dado que se forman dos moles de gliceraldehído 3-fosfato a partir de un mol de glucosa, se generan dos NADH en este paso
Paso 7- Transferencia de fosfato de 1,3-difosfoglicerato a ADP

- Este paso es el paso de la glucólisis que genera ATP.
- Implica la transferencia del grupo fosfato del 1,3-bisfosfoglicerato al ADP por la enzima fosfoglicerato quinasa, produciendo así ATP y 3-fosfoglicerato.
- Dado que se forman dos moles de 1,3-bisfosfoglicerato a partir de un mol de glucosa, se generan dos ATP en este paso.
Paso 8- Isomerización de 3-fosfoglicerato
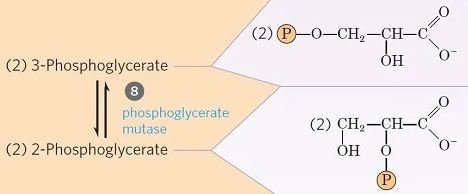
- El 3-fosfoglicerato se convierte en 2-fosfoglicerato debido al desplazamiento del grupo fosforilo de C3 a C2, por la enzima fosfoglicerato mutasa.
- Esta es una reacción de isomerización reversible.
Paso 9- Deshidratación 2-fosfoglicerato

- En este paso, el 2-fosfoglicerato se deshidrata por la acción de enolasa (fosfopiruvato hidratasa) a fosfoenolpiruvato.
- Esta es también una reacción irreversible en la que se pierden dos moles de agua.
Paso 10- Transferencia de fosfato de fosfoenolpiruvato

- Este es el segundo paso de la glucólisis que genera energía.
- El fosfoenolpiruvato se convierte en una forma enólica de piruvato por la enzima piruvato quinasa.
- El enol piruvato, sin embargo, se reorganiza rápidamente y de forma no enzimática para producir la forma ceto de piruvato (es decir, cetopiruvato). La forma ceto predominante a pH 7,0.
- La enzima cataliza la transferencia de un grupo fosforilo del fosfoenolpiruvato al ADP, formando ATP.
Importancia de la glucólisis
Es una vía importante para derivar energía en forma de ATP tanto aeróbicamente como anaeróbicamente, que es requerida por todas las células para realizar funciones celulares. Es una vía metabólica importante.
El proceso de glucólisis no requiere oxígeno. La omnipresencia de esta vía muestra que es una vía metabólica antigua y que ha evolucionado hace mucho tiempo.
Esta vía es utilizada por todas las células y tejidos para obtener energía, que se almacena en forma de ATP y NADH.
Ocurre tanto en procariotas como en eucariotas.
Se emplea tanto en la respiración aeróbica como en la anaeróbica.
El proceso de glucólisis ocurre en el citosol, por lo que es un proceso de generación de energía muy importante para aquellos organismos que no poseen mitocondrias.
El producto final de la glucólisis es el piruvato, que es un intermedio de varios otros procesos como la gluconeogénesis, la síntesis de ácidos grasos, la fermentación, etc.
Incluso los intermedios del proceso de glucólisis se utilizan en otras vías metabólicas, por ejemplo, DHAP (fosfato de dihidroxiacetona) se reduce para dar 3-fosfato de glicerol, que se utiliza en la formación de triglicéridos.
La glucólisis se interconecta con otros procesos como la fermentación del lactato y etanol, la transaminación para formar alanina, la vía de las pentosas fosfato, el metabolismo del glucógeno, etc.
Cuando hay una gran demanda de energía en los músculos y hay un suministro insuficiente de oxígeno, se utiliza la vía de glucólisis anaeróbica para generar energía.
Los eritrocitos obtienen energía de la fermentación del ácido láctico, ya que carecen de mitocondrias. El cristalino del ojo es otro ejemplo de glucólisis anaeróbica.
Como la mayoría de las reacciones son reversibles, la glucosa se genera a partir del piruvato mediante el proceso de gluconeogénesis.
Descripción general de la glucólisis
La glucólisis es una serie de reacciones enzimáticas que ocurren en el citoplasma. También se conoce como vía EMP (vía Embden Meyerhof Parnas).
Es el primer paso en la respiración celular. Las plantas y los animales obtienen energía de la descomposición de los carbohidratos. La sacarosa almacenada en las plantas se convierte en glucosa y fructosa. Estos monosacáridos entran en la vía glucolítica para generar energía.
Se producen dos moléculas de piruvato por oxidación parcial de glucosa.
¿Cuáles son las dos fases principales de la glucólisis?
Hay dos fases; Fase preparatoria, donde se consume ATP y fase de pago donde se produce ATP. Hay un rendimiento neto de 2 ATP y 2 NADH.
Es una serie de diez reacciones enzimáticas, donde la glucosa 6C se convierte en 2 moléculas de piruvato 3C.
1. Primera fase de la glucólisis
La glucosa se fosforila para formar fructosa-1,6-bisfosfato en el proceso de tres pasos y luego se descompone en el compuesto 3C G3P (gliceraldehído-3-fosfato) y DHAP (dihidroxiacetona fosfato). Este último genera G3P. En esta fase se utilizan 2 ATP.
2. Segunda fase de la glucólisis
Es una fase de captura de energía, G3P se convierte en piruvato en cinco pasos. Aquí obtenemos 4 ATP y se forman 2 NADH.
El piruvato ingresa a las mitocondrias en la respiración aeróbica eucariota, donde sufre una descarboxilación oxidativa para formar acetil CoA, que ingresa al ciclo de Krebs o al ciclo del ácido cítrico.
En los procariotas aeróbicos, esta reacción tiene lugar en el citosol.
El piruvato se convierte en lactato en la respiración anaeróbica, por ejemplo, en los músculos o acetaldehído, que se convierte en etanol y CO 2 en bacterias y levaduras.
¿Qué es la glucólisis aeróbica?
La glucólisis aeróbica es el proceso de oxidación de la glucosa en piruvato seguido de la oxidación del piruvato en CO 2 y H 2 O en presencia de una cantidad suficiente de oxígeno.
¿Qué es la glucólisis anaeróbica?
La glucólisis anaeróbica es el proceso que tiene lugar en ausencia de suficiente oxígeno, lo que resulta en la reducción del piruvato en lactato y la reoxidación de NADH en NAD + .
¿Dónde ocurre la glucólisis?
La glucólisis ocurre en la fracción extramitocondrial de la célula en el citosol.
¿Cuáles son los productos de la glucólisis?
Los productos de la glucólisis son dos moles de piruvato, cuatro moles de ATP (ganancia neta de 2 ATP) y un mol de NADH.
¿Cuántos NADH se producen por glucólisis?
La glucólisis produce dos moles de NADH.
¿Cuántos ATP se forman en la glucólisis?
En la glucólisis se forman un total de cuatro moles de ATP. La ganancia neta de ATP en la glucólisis es de solo 2 ATP, ya que se utilizan dos ATP durante la fase preparatoria de la glucólisis.
¿Cuáles son las funciones de la glucólisis?
La función principal de la glucólisis es producir energía en forma de ATP. De manera similar, la glucólisis también produce piruvato, que luego se oxida más para crear más ATP.
El camino Embden-Meyerhof-Parnas
La glucólisis se puede definir ampliamente como una vía de producción de energía que da como resultado la escisión de una hexosa (glucosa) en una triosa (piruvato).
Aunque el término a menudo se considera sinónimo de la vía Embden-Meyerhof-Parnas (EMP), existen otras vías glucolíticas, entre ellas la vía Entner-Doudoroff que procede a través de un intermedio de ácido glucónico y un conjunto complejo de reordenamientos que proceden a través de un pentosa intermedia
La vía EMP está presente en organismos de todas las ramas de las bacterias, arqueas y eucarias.
Claramente, esta es una adaptación evolutiva temprana, probablemente presente en el antepasado de todas las formas de vida actuales. Esto sugiere que la vía EMP evolucionó en un mundo fermentativo anaeróbico.
Sin embargo, la vía también funciona de manera eficiente como base para la respiración aeróbica de glucosa. Las diferencias entre la fermentación y la respiración radican principalmente en los diferentes destinos del piruvato producido (ver más adelante).
Para simplificar, esta discusión se centra en la vía EMP en la conocida bacteria Escherichia coli , aunque las características básicas de la vía son casi universales.
Antes de que comience el metabolismo de la glucosa, debe transportarse al interior de la célula y fosforilarse.
En E. coli , estos dos procesos están íntimamente acoplados de modo que la glucosa es fosforilada por el sistema de fosfotransferasa (PTS) a medida que pasa al interior de la célula.
Dado que la glucosa-6-fosfato (G-6-P), como la mayoría, si no todos, los fosfatos de azúcar , es tóxica a altas concentraciones celulares, este proceso de transporte está estrictamente regulado.
La transcripción del gen transportador específico de glucosa , ptsG , es máxima sólo cuando se acumula el monofosfato de adenosina cíclico (cAMP) (limitación de la energía de señalización).
Además, la traducción de ptsG El ARN mensajero (ARNm) es inhibido por el ARN pequeño sgrS , que se produce cuando se acumula G-6-P. Por lo tanto, la importación y la fosforilación concomitante a G-6-P se reduce cuando la demanda de más energía es baja o la concentración de G-6-P es peligrosamente alta.
En ausencia de una proteína PtsG, otros transportadores ligados a PTS, especialmente el transportador específico de manosa, ManXYZ, también pueden transportar y fosforilar glucosa.
Sin embargo, los mutantes de ptsG crecen más lentamente con glucosa que con cepas de tipo salvaje. La glucosa libre también puede acumularse intracelularmente a partir de la degradación de oligosacáridos que contienen glucosa , como lactosa o maltosa.
La entrada de glucosa intracelular en la vía EMP se produce a través de una hexoquinasa codificada por el gen glk.
Los siguientes dos pasos en la vía EMP preparan el G-6-P para la escisión en dos triosa fosfatos. Primero, una fosfoglucosa isomerasa reversible ( gen pgi ) convierte G-6-P en fructosa-6-fosfato.
Un mutante pgi todavía puede crecer lentamente con glucosa mediante el uso de otras vías glucolíticas (ver más adelante), pero la vía EMP está bloqueada en un mutante pgi.
La fructosa-6-fosfato resultante se fosforila adicionalmente en la posición C1 a fructosa-1,6, -bisfosfato a expensas del trifosfato de adenosina (ATP) por una fosfofructoquinasa codificada por pfkA.
Una segunda isoenzima menorde fosfofructoquinasa codificada por pfkB permite el crecimiento lento de mutantes pfkA.
Un conjunto potencialmente competitivo de fosfatasas que eliminan el fosfato C1 de la función fructosa-1,6, -bisfosfato durante la gluconeogénesis, pero que se controlan durante la glucólisis mediante una variedad de mecanismos de retroalimentación para prevenir ciclos inútiles.
La siguiente reacción en la vía es la escisión de fructosa-1,6-bisfosfato en dos triosa fosfatos que le dan a la vía su nombre ( glucólisis = rotura del azúcar).
Esta reacción reversible es llevada a cabo por la fructosa bisfosfato aldolasa ( gen fbaA ) y produce dihidroxiacetona fosfato (DHAP) y gliceraldehído fosfato (GAP) como productos.
Una segunda aldolasa no relacionada ( gen fbaB ) se produce solo durante la gluconeogénesis y, por lo tanto, no desempeña ningún papel en la glucólisis.
Los dos fosfatos de triosa son libremente interconvertibles a través de la triosafosfato isomerasa ( gen tpi ). DHAP es un sustrato clave para los lípidos biosíntesis.
GAP es un nodo importante en la glucólisis; otras dos vías glucolíticas comunes (ver más abajo) se unen a la vía EMP en GAP.
Hasta este punto, la vía EMP se puede considerar como una vía biosintética ya que produce tres bloques de construcción biosintéticos clave (G-6-P, fructosa-6-fosfato y DHAP) a expensas del ATP y sin pasos oxidativos.
El siguiente paso es la fosforilación oxidativa de GAP a ácido 1,3-difosfoglicérico, un compuesto de alta energía. La incorporación de fosfato inorgánico por GAP deshidrogenasa ( gen gapA ) está acoplada a la reducción de NAD + a NADH.
En condiciones aeróbicas, este NADH se reoxida utilizando la cadena respiratoria.para producir ATP. En condiciones anaeróbicas, este NADH se reoxida al acoplarse a la reducción de productos derivados del piruvato u otros intermedios de la vía EMP.
La enzima fosfoglicerato quinasa ( gen pgk ) luego fosforila el difosfato de adenosina (ADP) a ATP a expensas del fosfato C1 del 1,3-difosfoglicerato.
Esta es la primera de dos fosforilaciones a nivel de sustrato donde el fosfato se transfiere de un sustrato altamente reactivo directamente al ADP sin la participación de la ATP sintasa de membrana .
Los siguientes dos pasos reorganizan el 3-fosfoglicerato resultante en el último intermedio de alta energía de la vía, el fosfoenolpiruvato (PEP). Primero, el fosfato se transfiere de la posición C3 a la posición C2 mediante una fosfoglicerato mutasa.
Hay dos isoenzimas evolutivamente no relacionadas, una de las cuales (codificada por el gen gpmA ) requiere un 2,3-bisfosfoglicerato como cofactor y la otra ( gen gpmM ) no. Aunque E. coli, Bacillus subtilis y algunas otras bacterias tienen ambas isoenzimas, muchos organismos solo tienen una u otra.
Por ejemplo, la levadura Saccharomyces cerevisiae , la bacteria Mycobacterium tuberculosis, y todos los vertebrados tienen solo la enzima dependiente del cofactor, mientras que las plantas superiores, las arqueas y la bacteria Pseudomonas syringae tienen solo la enzima independiente del cofactor.
Una tercera isoenzima ( gen ytjC ) parece existir en E. coli , aunque su función es menos clara.
El 2-fosfoglicerato reordenado es luego deshidratado por una enolasa ( gen eno ) para producir el intermedio clave, PEP. Aunque generalmente se considera que el piruvato es el producto final de la vía EMP, se puede argumentar que PEP comparte ese honor.
La PEP es la fuente última de fosfato para el transporte / fosforilación de glucosa mediado por PtsG que inicia la vía. Además, la enzima enolasa es una parte necesaria del degradasoma que funciona con el ARN pequeño sgrS (descrito anteriormente) para inhibir la traducción del ARNm de ptsG y estimular la degradación del ARNm de ptsG. Esto reduce la generación de la acumulación tóxica de G-6-P.
Vale la pena señalar que la PEP es un punto de ramificación tanto en condiciones aeróbicas como anaeróbicas.
La carboxilación de PEP por la PEP carboxilasa ( gen ppc ) proporciona oxaloacetato , que se condensa con el acetil-CoA derivado del piruvato para formar citrato para ejecutar tanto el ciclo del ácido tricarboxílico (TCA) como la derivación del glioxilato de forma aeróbica.
Durante la fermentación, este mismo oxalacetato es un intermedio en la vía reductora (regeneradora de NAD) para succinato.
Además, el oxalacetato derivado de la PEP se utiliza (a través de una parte del ciclo del TCA) para la biosíntesis del ácido glutámico. incluso en condiciones anaeróbicas.
La última reacción es una fosforilación a nivel de sustrato de ADP a ATP a expensas de PEP para producir piruvato. Las dos isoenzimas de la piruvato quinasa ( genes pykA y pykF ) son activadas por azúcares fosfatos y el producto del gen pykF muestra cooperatividad positiva con respecto al sustrato PEP, de nuevo tendiendo a prevenir la acumulación de este intermedio fosforilado y evitando así la generación de más G-6-P a través del mecanismo de transporte de PtsG dependiente de PEP.
Al final de la vía EMP, 1 mol de glucosa se convierte en 2 mol de piruvato, que puede usarse para un mayor catabolismo o para la biosíntesis. También produce 2 mol de ATP y 2 mol de NADH (que deben reoxidarse para que la vía continúe funcionando).
Dado que la vía genera varios intermedios tóxicos, no es sorprendente que el flujo a través de la vía esté estrictamente regulado.
Las enzimas de la vía responden rápidamente a las variaciones en la oferta y la demanda mediante la inhibición por retroalimentación y la activación del sustrato de las actividades enzimáticas.
También responden (más lentamente) mediante la regulación transcripcional de la expresión génica en respuesta a reguladores globales que varían de un organismo a otro.
La vía EMP funciona para generar tanto intermedios biosintéticos como energía catabólica a partir de la glucosa. Sin embargo, también sirve como una línea troncal central en la que se alimentan muchas otras vías catabólicas.
G-6-P, fructosa-6-fosfato, DHAP y GAP son puntos de unión comunes donde las vías catabólicas para azúcares, alcoholes, grasas y ácidos orgánicos se introducen en la vía EMP.
▶️ Índice:





